Nous développons actuellement plusieurs axes de recherche :
Caractérisation des mécanismes d’oncogenèse et développement de nouvelles approches thérapeutiques dans le lymphome NK/T
Les lymphomes NK/T extra-ganglionnaires de type nasal sont des entités rares et graves de lymphomes T périphériques associées au virus d’Epstein Barr, dont l’oncogenèse reste encore mal élucidée à ce jour.
Notre recherche sur le lymphome NK/T repose sur une collaboration étroite avec les Pr Hermine et Jaccard, cliniciens experts dans cette pathologie. Les nouveaux cas sont identifiés par le biais d’une Réunion de Concertation Pluridisciplinaire (RCP) nationale dédiée aux lymphomes NK/T, à laquelle Lucile Couronné participe activement. L’équipe collabore également de manière rapprochée avec le réseau LYSATOMIC du LYSA pour centraliser les échantillons des patients et recueillir les données cliniques associées.
Comprendre les mécanismes d’échappement tumoral associé au lymphome NK/T
Il est connu que l’infection des cellules B par l’EBV peut conduire à une prolifération incontrôlée des cellules infectées puis au développement de lymphomes chez les sujets immunodéficients. Or les patients avec lymphome NK/T ne présentent en général pas de déficit immunitaire primaire, suggérant que d’autres mécanismes d’échappement à la réponse immune anti-EBV et plus largement, anti-tumorale sont impliqués dans la lymphomagenèse NK/T. Plusieurs mécanismes ont déjà été rapportés dont la surexpression du checkpoint immunitaire PD-L1 par les cellules tumorales de lymphome NK/T ou la présence de la présence de mutations dans des gènes impliqués dans la surveillance immunitaire.
Notre équipe cherche à comprendre les mécanismes intrinsèques et extrinsèques associés à l’échappement tumoral dans les lymphomes NK/T.
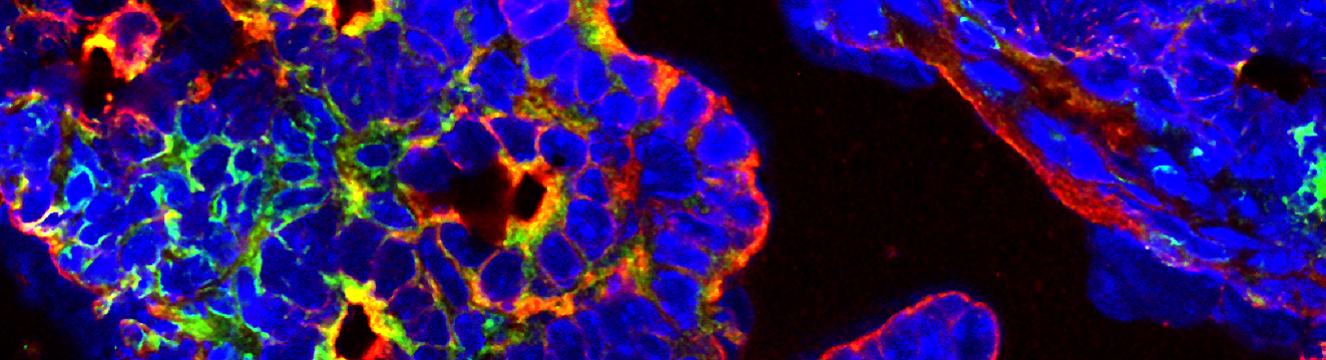
Pour répondre à cet objectif, nous utilisons des modèles de réponse immune in vitro et in vivo basés sur des lignées cellulaires et/ou des cellules primaires de patients. Nous visons également à caractériser le microenvironnement tumoral des échantillons de lymphomes NK/T à l’aide d’approches avancées telles que l’immunofluorescence multiplex et la transcriptomique spatiale.
Identifier des facteurs de réponse aux immunothérapies dans le lymphome NK/T
Pour améliorer l'immunité anti-tumorale, les inhibiteurs de PD-1 (aPD1) ont été évalués chez les patients en rechute/réfractaires et/ou à un stade avancé, avec une efficacité prometteuse, bien que partielle.
Nous cherchons à identifier des biomarqueurs prédictifs de la réponse aPD1 par une approche multi-omique reposant sur le profilage des échantillons tumoraux à l’aide de techniques de pointe, telles que le séquençage de nouvelle génération, la cartographie optique du génome, l’immunofluorescence multiplex, la transcriptomique spatiale ou encore l’analyse du méthylome. En complément, nous analyserons le statut immunitaire des patients via des approches telles que la cytométrie de masse, le scRNA-seq et l’analyse du répertoire T, afin d’obtenir une vue intégrée et détaillée de la réponse immunitaire.
Développer de nouvelles approches thérapeutiques dans le lymphome NK/T
Le pronostic des patients en rechute ou réfractaires et des formes disséminées demeure sombre. Nous souhaitons donc développer de nouvelles approches thérapeutiques, en monothérapie ou en combinaison, avec un intérêt particulier pour les thérapies immunomodulatrices et celles présentant une synergie avec les aPD1. Dans ce cadre, nous établissons des partenariats industriels pour évaluer de nouvelles molécules prometteuses. Par ailleurs, nous travaillons à la création de modèles précliniques innovants, incluant des modèles murins et non murins (organoïdes), afin d’évaluer l’efficacité de ces approches thérapeutiques dans des contextes expérimentaux pertinents.
Etude de la physiopathologie des lymphoproliférations T digestives de bas grade
Le lymphome T indolent du tractus gastrointestinal est une pathologie très rare (moins de 70 cas rapportés dans la littérature), se caractérisant par des lésions multifocales du tube digestif, principalement dans l'intestin grêle et le côlon, avec une infiltration clonale de l’épithélium et du chorion par des cellules T de petite taille, le plus souvent CD4+. Bien que généralement indolente, elle peut entraîner des symptômes digestifs persistants et une altération de la qualité de vie. Dans de rares cas, elle peut évoluer vers un lymphome agressif plusieurs années après le diagnostic. Le diagnostic est complexe, et aucune stratégie thérapeutique conventionnelle n'est efficace. En raison de la rareté de cette maladie chez l’homme, nous avons étudié un modèle animal félin spontané, le lymphome digestif de bas grade à petites cellules T du chat (LGITL) grâce à une collaboration avec l’école nationale vétérinaire d’Alfort (Dr Valérie Freiche). Nos données indiquent que les caractéristiques du LGITL sont très similaires à celles de la GI-TLPD humaine et valident que ce modèle animal est pertinent pour l’étude de la maladie chez l’homme. Nous avons en outre mis en évidence une dérégulation de la voie JAK/STAT (surexpression de Phospho-STAT5) lors de LGITL qui pourrait représenter une cible thérapeutique d’intérêt, commune aux deux espèces.
En raison du caractère fortement émergent de l’entité féline, approfondir les connaissances sur le LGITL pourrait offrir une perspective importante pour mieux caractériser la maladie humaine, en particulier pour tester des inhibiteurs de l'axe JAK/STAT.
Afin de mieux comprendre l’oncogenèse moléculaire de ces lymphomes, nous avons réalisé des analyses pan-génomiques et -transcriptomiques sur un groupe de 20 chats atteints de LGITL. Actuellement, nous menons des études fonctionnelles pour explorer le rôle de certains gènes candidats dans la pathogenèse de ces lymphomes et évaluer leur récurrence chez l’homme
Caractérisation moléculaire des lymphomes B associés aux déficits immunitaires
Les déficits immunitaires héréditaires (DIH) constituent un groupe hétérogène de maladies, souvent diagnostiquées dans l'enfance, qui prédisposent au développement de lymphomes. Le paysage génétique des lymphomes associés aux DIH est mal connu. Leur traitement n’est pas codifié et représente un défi en raison d'une toxicité accrue des chimiothérapies chez ces patients. Par ailleurs, la survenue du lymphome peut constituer la première manifestation d’un DIH sous-jacent non diagnostiqué jusqu’alors.
Nous souhaitons donc caractériser, sur le plan moléculaire, les lymphomes associés aux DIH. Dans le cadre d’une collaboration avec les services d’immuno-hématologie pédiatrique et d’hématologie adulte de l’hôpital Necker et le département de pathologie de l’hôpital Necker, nous étudierons une cohorte d’environ 200 lymphomes B, adultes et pédiatriques, cliniquement annotée et revue histologiquement, survenus chez des patients présentant un DIH bien caractérisé. Cette analyse s'appuiera sur une approche pan-omics intégrative pour identifier des signatures spécifiques à différents types de DIH.
Une analyse comparative sera également menée avec les lymphomes survenant chez des patients immunocompétents, dans le but d’identifier des biomarqueurs cliniques, biologiques, histologiques et moléculaires susceptibles d’indiquer la présence d’un DIH sous-jacent.
En parallèle, nous souhaitons explorer le paysage génétique des lymphomes B pédiatriques survenant en post-transplantation dans un contexte de déficit immunitaire acquis. Cette étude visera à mieux comprendre la pathogenèse de ces lymphomes et à identifier des facteurs pronostiques ou prédictifs de réponse au traitement, permettant ainsi d’améliorer la prise en charge thérapeutique.
La caractérisation moléculaire des lymphomes associés aux déficits immunitaires, qu’ils soient primitifs ou acquis, devrait non seulement permettre d’éclairer les mécanismes de lymphomagénèse dans un contexte de défaut immunitaire spécifique, mais aussi contribuer à une meilleure compréhension des lymphomes survenant chez les patients immunocompétents, tout en révélant de potentielles cibles thérapeutiques innovantes.